Информация о препарате CR 173487 для специалистов
Исследования препарата
Исследования препарата CR 173487 проводятся в ведущих НИИ Украины и в медицинских учреждениях на предмет переносимости, безопасности, терапевтического действия, фармакокинетических и фармакодинамических характеристик, терапевтических уровней дозирования, изучения способов введения, формирования протоколов лечения в соответствии с поставленным диагнозом.
I фаза исследований, 2007-2009гг.
| Предметы изучения | Диагнозы | Мед. учреждение/ руководитель исследований | Лекарственная форма |
Переносимость Острая токсичность препарата | Опухоли головного мозга: ● Анапластическая олигодендроастроцитома ● Анапластическая астроцитома ● Эпендимома ● Глиосаркома ● Глиобластома | Главный онконейрохирург НАМН Украины, руководитель отдела нейроонкологии и нейрохирургии детского возраста Института нейрохирургии имени Академика А.П. Ромоданова НАМН Украины, член-корреспондент НАМН Украины, профессор, д.м.н., Розуменко Владимир Давидович | Раствор для инъекций |
Исследования позволили сделать предварительные выводы о противоопухолевой активности препарата:
- клиническое торможение опухолевого процесса
- процесс лечебного апоптоза
- улучшение качества жизни
С 2018 года клинические исследования препарата проводятся по ряду агрессивных опухолей:
| Внутримозговые опухоли | Опухоли желудочно-кишечного тракта (ЖКТ) | Опухоли эндокринной системы | Рак легких |
Благодаря расширенным исследованиям I-й фазы клинических исследований, зафиксированы и утверждены:
- максимально допустимые дозы препарата (переносимость)
- дозировки лекарств, необходимые для лечения того или иного вида рака
- способ введения препарата (форма применения)
II фаза клинических исследований
II фаза контролируемых рандомизированных клинических исследований показала высокую эффективность препарата, позволила составить предварительные протоколы лечения в зависимости от диагноза и других важных показателей.
III фаза многоцентровых клинических исследований
Активно проводится в настоящее время и характеризуется положительными качественными результатами.
Результаты уже проведённых исследований указывают на нетоксичность и безопасность препарата. Другими словами, препарат не оказывает токсического действия на организм человека. Его использование является безопасным для пациента, факты прямого токсического воздействия препарата на организм человека до настоящего времени не зафиксированы.
Реакция на введение препарата часто проявляется незначительным повышением температуры тела пациента в первые 3-5 дней после введения препарата, что свидетельствует об ответной реакции иммунной системы организма и не требует специального лечения.
По результатам проведённых исследований представляется возможным сделать предварительные выводы о противоопухолевой активности препарата: установлено клиническое торможение опухолевого процесса, что свидетельствует в пользу лечебного патоморфоза и приводит к улучшению качества жизни (согласно опросникам ВОЗ).
Привыкание к препарату не зафиксировано.
Препарат CR 173487 способен ввести в длительную ремиссию, излечить больного.
Особенности применения препарата
Применение препарата позволяет улучшить состояние здоровья практически всех онкобольных, так как уже в течение первых двух-трёх недель со дня начала лечения в организме больного наблюдается разрушение значимой части опухолевых клеток.
Продолжительность лечения препаратом
Продолжительность лечения препаратом, включая процессы реабилитации (выведение и резорбцию разрушенных клеток, восстановление надлежащих функций организма больного), зависит от характера и степени тяжести заболевания. Для больных, ослабленных приёмом ранее используемых высокотоксичных лекарств и процедур и имеющих несколько зон онкологического поражения, процесс лечения препаратом является поэтапным и более длительным. Конкретная продолжительность курса лечения, дозы и способы введения препарата зависят от локализации, гисто и цитогенеза злокачественной опухоли.
В период лечения препаратом необходим постоянный клинический контроль здоровья пациента. Важно исключить не согласованные к применению другие лекарственные средства, в том числе на спиртовой основе. Препарат нельзя применять одновременно с лучевой и химиолучевой терапией, так как эти методики значительно увеличивают уровень токсичных веществ в организме больного, угнетают его иммунную систему, отрицательно влияют на возможности организма в регенерации тканей, нивелируют действие препарата. Интервал между приемом препарата CR 173487 и другими методами воздействия на опухоль (химиотерапия, лучевая терапия) должен составлять не менее 7 дней.
Диетическая добавка ТИОСАН® – новые возможности для пациентов.
В 2016 году фармацевтическая компания КРАУН ФАРМА зарегистрировала новый продукт – диетическую добавку ТИОСАН, который предназначен для перорального применения и используется в качестве средства для оптимизации лечения злокачественных новообразований (заключение государственной санитарно-эпидемиологической экспертизы №602-123-29-2/2525 от 05.12.2016 г., ТУ У 10.8-40893378-001:2016; протокол исследований № 3/8-А-3811-17-64752Е от 31.07.2017г.).
С декабря 2017 года по настоящее время в Институте нейрохирургии имени Ромоданова НАМН Украины проводятся клинические исследования по применению диетической добавки ТИОСАН у пациентов с установленным диагнозом глиобластома и/или анапластическая глиома (2 протокола клинических исследований).
| Предмет изучения | Диагноз | Медицинское учреждение/руководитель исследований | Лекарственная форма |
| Переносимость и эффективность | ● глиобластома ● анапластическая глиома (анапластическая астроцитома, анапластическая олигодендроглиома, анапластическая олигоастроцитома) | Главный онконейрохирург НАМН Украины, руководитель отдела нейроонкологии и нейрохирургии детского возраста Института нейрохирургии имени Академика А.П. Ромоданова НАМН Украины, член-корреспондент НАМН Украины, профессор, д.м.н., Розуменко Владимир Давидович | Раствор для перорального применения |
Предварительные результаты свидетельствуют о положительном влиянии данного продукта на ход лечения внутримозговых онкозаболеваний III и IV степени злокачественности.
ТИОСАН улучшает качество жизни пациентов, не вызывает побочной симптоматики, проявления токсичности не наблюдались.
Реакция на продукт часто проявляется незначительным повышением температуры тела пациента в первые 3 — 5 дней после приема, что свидетельствует об ответной реакции иммунной системы организма и не требует специального лечения.
Привыкание к продукту до настоящего времени не зафиксировано.
ТИОСАН безвреден в применении.
Накапливаются данные о его эффективности.
ТИОСАН может применяться при лечении различных онкологических процессов.
Применение препарата целесообразно как на ранних стадиях рака, так и на более поздних, когда подключается процесс метастазирования.
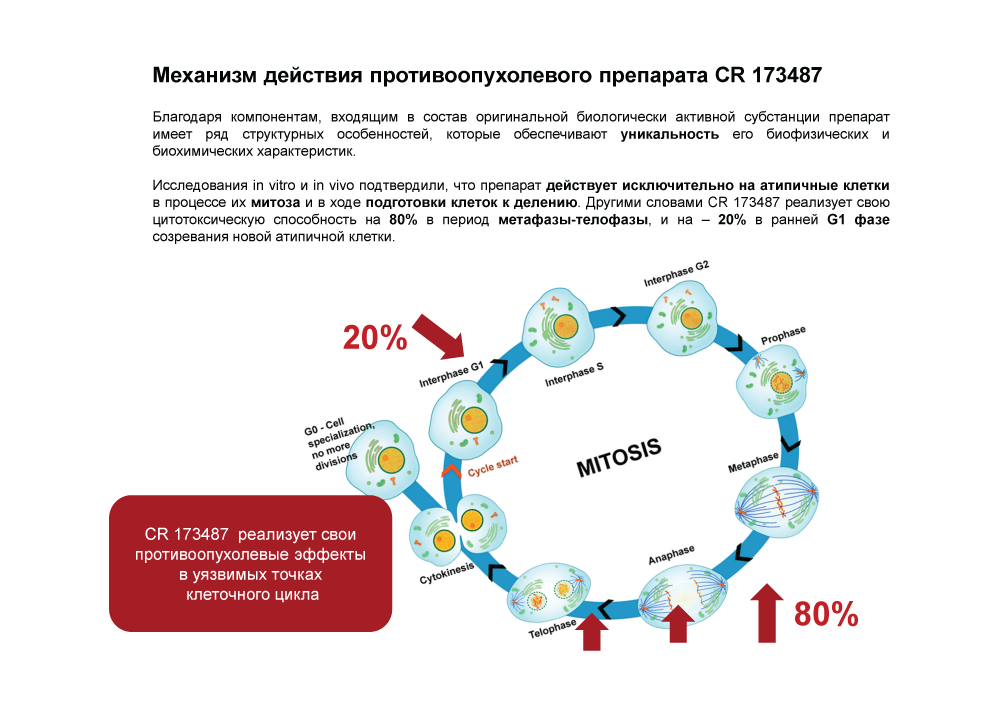
Противоопухлевое действие препарата реализуется в период размножения атипичных клеток преимущественно посредством блокирования митоза. В результате нежизнеспособные клетки подвергаются лечебному патоморфозу и утилизируются макрофагами.
Так достигается контроль над заболеванием даже на поздних стадиях.